SARS-CoV-2 zwiększa wiek biologiczny [1],[2]
Xavier Azalbert, Anne-Typhaine Bouthors, Michel Brack, Dominique Cerdan, Walter Chesnut, Gérard Guillaume, Jean-François Lesgards, Luc Montagnier, Jean-Claude Perez
Tłumaczenie z francuskiego prof. Jakub Z. Lichański, korekta Weronika Kokot.
Czy znasz określenie „starzenie się”? W biologii jest to proces fizjologiczny, który z czasem prowadzi do upośledzenia funkcjonowania komórki. Naukowcy od zawsze starali się ograniczyć starzenie się, mając w pamięci chińskie przysłowie cytowane przez Malraux:
„Musimy dodać życie do lat, a nie lata do życia”.
Kilka ostatnich badań pokazuje, że SARS-CoV-2 zwiększa biologiczny wiek komórek. Jak? Działając na długość telomerów, sekwencji DNA chroniących końce chromosomów i skracających się z każdym podziałem komórki.
W kwietniu 2021 r. chińscy badacze, Yuyang Lei i Jiao Zhang, opublikowali w Circulation Research artykuł, w którym wykazali, że głównym patogenem wirusa Covid-19 jest jego białko kolca, zwane Spike. Białko kolca otacza kapsyd wirusa i pozwala mu wniknąć do komórek, aby je zakazić. W tym badaniu wszczepiono chomikom syryjskim niezakaźną i niezawierającą w kapsydzie całego materiału genetycznego wirusa SARS-CoV-2 sztucznie wytworzoną strukturę, zdolną jednak do ekspresji białka kolca, aby obserwować działanie samego białka kolca na organizm. U badanych zwierząt wystąpiły uszkodzenia płuc i tętnic związane z zapaleniem komórek śródbłonka. Zespół powtórzył eksperyment in vitro na zdrowych ludzkich komórkach śródbłonka – okazało się, że białko kolca wiąże się z receptorami ACE2, uszkadzając mitochondria komórek, powodując mikrozakrzepy i zapalenie śródbłonka. Wnioski są jasne: samo białko kolca powoduje większość objawów Covid-19 (więcej o Covid-19 w dalszej części artykułu).
Natychmiast nasuwa się kilka pytań:
- Jeśli zostanie udowodnione, że SARS-CoV-2 przyspiesza starzenie się komórek, a za to starzenie odpowiada białko kolca, jak możemy mieć absolutną pewność, że obecnie dostępne na rynku szczepionki, wszystkie oparte na tym białku, również nie prowadzą do przyspieszonej degradacji komórek zaszczepionych osób?
- Jakie są powiązania między mechanizmami starzenia się związanymi ze skracaniem telomerów a szczepionkami?
Kilka odpowiedzi znajduje się w tym artykule. Ostrzegamy czytelnika, że zrozumienie niektórych akapitów wymaga pewnej wiedzy z biologii lub biochemii. Wnioski z lektury przeznaczone są jednak dla ogółu społeczeństwa.
Przyspieszenie starzenia się
W listopadzie 2020 r. zespół naukowców z Cliniques Universitaires Saint-Luc i UC Louvain zbadał potencjalną rolę telomerów w zakażeniu Covid-19. Wiek, otyłość, cukrzyca, nadciśnienie i wiele czynników warunkujących ciężkość przebiegu choroby są obecnie dobrze zidentyfikowanymi prognostykami powikłań. Jednak także pacjenci, którzy nie spełniają tych kryteriów, czasami cierpią z powodu ciężkiego przebiegu tej choroby.
Telomery i ich rola
Artykuł przeglądowy z tej samej uczelni wyjaśnia, czym są telomery i jaka jest ich rola.
- Telomery to sekwencje DNA, które chronią końce chromosomów i skracają się przy każdym podziale komórki. Ich długość zmniejsza się wraz z wiekiem komórki i osobnika. Kiedy stają się zbyt krótkie, zwłaszcza u osób starszych, komórki starzeją się, a zjawisko to zwiastuje śmierć komórki. Struktury te pełnią zatem rolę komórkowego zegara biologicznego.
- Wielu naukowców wykazało, że skracanie telomerów zmniejsza oczekiwaną długość życia.
- Jednak długość telomerów nie jest taka sama dla wszystkich osobników w tym samym wieku i ma na nią wpływ między innymi zmienność genetyczna. Wydaje się, że skrócenie telomerów wpływa na zdolność obrony organizmu przed wirusami – uważa się, że osoby z krótszymi telomerami szybciej wyczerpują zapasy komórek odpornościowych.
- Aby lepiej zrozumieć mechanizmy odpornościowe związane z Covid-19 profesorowie Froidure (Wydział Pulmonologii) i Decottignies zbadali potencjalny związek między długością telomerów a Covid-19. Badanie przeprowadzono u pacjentów hospitalizowanych z powodu Covid-19, prawie u wszystkich z brakiem limfocytów we krwi.
- Naukowcy porównali długość telomerów 70 pacjentów hospitalizowanych z powodu Covid-19 podczas pierwszej fali pandemii (od 7 kwietnia do 27 maja 2020 r., pacjenci w wieku od 27 do 96 lat) z wynikami grupy kontrolnej złożonej z około 500 osób niezakażonych Covid-19.
- Wyniki wykazały, że: i) telomery pacjentów zakażonych Covid-19 były krótsze niż w grupie kontrolnej oraz ii) obecność bardzo krótkich telomerów (poniżej 10. percentylu dla wieku) wiązała się ze znacznie wyższym prawdopodobieństwem wymagania opieki medycznej lub śmierci.
- Wyniki te rzucają nowe światło na mechanizmy warunkujące odporność na koronawirusa.
Wyniki potwierdzone i dopracowane w 2021 r.
W styczniu 2021 roku badaczka zajmująca się onkologią molekularną, Maria Blasco, potwierdziła wyniki Froidure et al. opublikowane w artykule zatytułowanym „Krótsze telomery u pacjentów z ciężką chorobą Covid-19”, który pozostał niezauważony. W podsumowaniu czytamy, że:
- zapadalność na Covid-19 o ciężkim przebiegu wzrasta z wiekiem i u starszych pacjentów obserwuje się najwyższą umieralność, co sugeruje że na ciężkość przebiegu Covid-19 wpływają molekularne mechanizmy odpowiadające za starzenie się. Autorzy przypominają, że „Jednym z mechanizmów starzenia się jest postępujące skracanie się telomerów, struktur ochronnych na końcach chromosomów. Skrajnie skrócone telomery upośledzają zdolność tkanek do odnowy, co skutkuje zaburzeniem homeostazy i chorobą. Wirus SARS-CoV-2 zakaża różne rodzaje komórek, zmuszając je do odnowy – tworzenia nowych komórek – w celu utrzymania homeostazy”.
- Autorzy postawili zatem hipotezę, że obecność krótkich telomerów u starszych pacjentów ogranicza odpowiedź tkankową na zakażenie SARS-CoV-2. Zmierzyli oni długość telomerów w limfocytach krwi obwodowej pacjentów z Covid-19 w wieku od 29 do 85 lat i odkryli, że krótsze telomery są związane z cięższym przebiegiem choroby.
Te badania nie uzyskały rozgłosu. Jako jeden z niewielu doniósł o nich Sante Log w artykule zatytułowanym nieśmiało „Co, jeśli Covid skraca telomery?”. Zanim sformułujemy wnioski, należy odpowiedzieć na pytanie, czy skrócenie telomerów oznacza przyspieszone starzenie się i skrócenie życia.
W maju 2021 r. w preprincie (Gorgoulis i wsp. 2021) stwierdzono, że SARS-CoV-2 zakaża komórki nabłonka płuc i indukuje starzenie się oraz reakcję zapalną u pacjentów z Covid-19 o ciężkim przebiegu.
Do czerwca 2021 r. udowodniono związek między skróceniem telomerów u pacjentów z Covid-19 a zwiększeniem wieku biologicznego (Gaetano i wsp.). Wnioski są jednoznaczne:
- Zakażenie SARS-CoV-2 powoduje zespół covidowy, który w najgorszym przypadku charakteryzuje się ciężką niewydolnością oddechową, zwłóknieniem płuc i serca, uwalnianiem cytokin prozapalnych i immunosupresją. Ten stan spowodował dotychczas śmierć około 2,15% zakażonej populacji na świecie.
- Wśród ozdrowieńców, PPCS (ang. persistent post-COVID-19 syndrome, zespół pocovidowy) wiąże się z jednym lub większą liczbą następujących objawów: zmęczeniem, dusznością, utratą pamięci, zaburzeniami snu i trudnościami z koncentracją. W badaniu zmierzono wiek biologiczny 117 osób, które przeszły Covid-19 i 144 niezakażonych ochotników.
- Autorzy zauważają znaczny przyrost wieku biologicznego pacjentów po przejściu Covid-19 (oznaczonych w poniższej tabeli jako „post-COVID-19”) wynoszący 10,45 lat (+/- 7,29 lub 5,25 lat powyżej normy) w porównaniu z 3,68 lat (+/- 8,17 lat) u osób niezakażonych (oznaczonych jako „sans COVID-19”).
Tabela 1 – Zestawienie danych
Tabela 2 – Rozkład zmiennej delta wieku (w latach)*

* Delta wieku oznacza różnicę pomiędzy wiekiem biologicznym a wiekiem kalendarzowym. W przypadku osób które przeszły covid, dystrybucja czerwonych punktów świadczy o statystycznie istotnym (p < 0,0001) przyroście wieku biologicznego czyli przyśpieszeniu starzenia w stosunku do osób, które nie zachorowały na covid (dystrybucja niebieskich punktów pokazuje kumulację delty wieku w zakresie + 3,68 lat).
- W kohorcie „post Covid-19” (3,03 kb) obserwuje się znaczące skrócenie telomerów w porównaniu z kohortą „sans Covid-19” (10,67 kb).
- Ponadto ekspresja ACE2 była zmniejszona o 73% u pacjentów po przejściu choroby w porównaniu z populacją nienarażoną na nią. Potwierdzają to dane z badania Butwot z maja 2020r. dotyczące ekspresji białek umożliwiających wejście SARS-CoV-2 do komórki – ACE2 i TMPRSS2 w nabłonku węchowym – typów komórek, wykazujących ekspresję tych białek oraz zmian w ich ekspresji wraz z wiekiem.
- W świetle tych obserwacji postawiono hipotezę, że pewne zmiany epigenetyczne są związane ze stanem po przejściu Covid-19, szczególnie u młodszych pacjentów (<60 lat).
Ostatnio w telewizji i na portalach społecznościowych pojawiły się liczne indywidualne wypowiedzi, które potwierdzają te fakty – nierzadko czyta się, słyszy lub zauważa, że ukochanej osobie „przybyło dziesięć lat” po ciężkim przejściu Covid-19. Ale, co bardziej niepokojące, te same doświadczenia spotykają również osoby zaszczepione.
Czym jest stres oksydacyjny i jaką rolę odgrywa w skracaniu telomerów i Covid-19?
Ostateczną przyczyną śmierci pacjentów chorujących na Covid-19 jest przewlekłe (przedłużające się) zapalenie, szczególnie poprzez aktywację krzepnięcia. To zapalenie, nazywane w uproszczony sposób „burzą cytokinową”, jest aktywowane przez cząsteczki (białka) zwane cytokinami. Cytokiny pełnią w ludzkim ciele rolę przekaźników międzykomórkowych, które wysyłają wiadomości, szczególnie w celu regulacji stanu zapalnego w narządach.
Temu zapaleniu komórek towarzyszą reakcje oksydacyjne bardzo reaktywnych, małych cząsteczek (zwanych wolnymi rodnikami), które są wytwarzane w miejscu zapalenia w procesie zwanym stresem oksydacyjnym. To tak, jakby stan zapalny był miotaczem ognia, a stres oksydacyjny płomieniem.
Te dwa ściśle ze sobą związane zjawiska (przewlekły stan zapalny i stres oksydacyjny) są podstawą większości chorób sercowo-naczyniowych (miażdżyca, zakrzepica itp.), chorób neurodegeneracyjnych (choroba Alzheimera, Parkinsona itp.), nowotworów, ale także starzenia.
A teraz okazuje się, że Covid-19 jest w rzeczywistości chorobą zapalną i oksydacyjną!
Kluczowe znaczenie stresu oksydacyjnego w patologii Covid-19 zostało w dużej mierze niedocenione i powinno być przedmiotem dodatkowych prac badawczych, w szczególności w celu identyfikacji terapii antyoksydacyjnych i przeciwzapalnych (Delgado-Roche L i in., 2020) (Cecchini R i al., 2020) (MP Ntyonga-Pono, 2020); jest to również ważne dla postępowania w przypadku przewlekłego Covid-19!
Zapalenie wywołane przez białko kolca w Covid-19 i związany z nim stres oksydacyjny w sposób szczególny zaburza działanie układu renina-angiotensyna-aldosteron [3]i aktywuje szlaki bradykininy (Lesgards JF., Cerdan D. 2021, artykuł przeglądowy dotyczący biologii SARS-CoV-2).
Wiele badań wykazało związek między stresem oksydacyjnym a skracaniem telomerów, a tym samym starzeniem się komórek i organizmu (Boonekamp JJ i in., 2017) (von Zglinicki T, 2002) (Kawanishi S i Oikawa, 2004) (Richter T i von Zglinicki T, 2007) (Griffin CS, 2002). Kilka badań wykazało również skrócenie telomerów wskutek działania dodanego utleniacza zużywającego glutation (głównego przeciwutleniacza organizmu) (Cattan V i wsp., 2008).
Ponadto w lipcu 2021 r., w populacji dobieranych losowo pacjentów hospitalizowanych z powodu Covid-19, powiązanie stresu oksydacyjnego z biomarkerami stanu zapalnego umożliwiło przewidzenie ciężkiego przebiegu choroby i konieczności hospitalizacji pacjentów na oddziale intensywnej terapii (Brack M. i wsp., 2021 ).
Stres oksydacyjny jest odpowiedzialny za skracanie telomerów w Covid-19
W utleniającym środowisku, powstającym podczas zakażenia komórki SARS-CoV-2 jednym z celów komórkowych Covid-19 są zasady budujące DNA oraz RNA, w szczególności cząsteczki guaniny (G). Głównym produktem utleniania występującej w organizmie guaniny jest 8-okso-7,8-dihydroguanina (8oksoG), która odgrywa ważną rolę w mutagenezie i karcynogenezie, czyli w wywoływaniu nowotworów (Fortini P i in., 2003). Jeśli następują po sobie w powtarzających się sekwencjach (GG..), co spotyka się w sekwencji genetycznej telomerów chroniących końce chromosomów, cząsteczki guaniny jeszcze łatwiej ulegają utlenieniu (Kino K i wsp., 2017). W normalnych warunkach organizm eliminuje te toksyczne produkty utleniania (8oxoG) za pomocą enzymu (glikozylazy OGG1) i naprawia uszkodzone DNA lub RNA. Ale telomery są bardzo bogate w guaninę i szczególnie wrażliwe na utlenianie, a produkcja istotnych ilości 8-oxoG skraca telomery i upośledza wzrost komórek (Fouquerel E i in., 2019) (von Zglinicki T i wsp., 2000). Ponadto telomery są naprawiane mniej wydajnie niż reszta genomu, ponieważ znajdują się na końcu chromosomów (Oikawa S i Kawanishi S, 1999) (Opresko Pl i wsp., 2005). Obecność 8-oksoG zmniejsza skuteczność telomerazy, enzymu, który naprawia telomery, powodując zakłócenia długości, utrzymywania i funkcjonalności telomerów (Opresko Pl i wsp., 2005). Uszkodzenia spowodowane nieprzekształconym z powrotem w guaninę 8-oksoG mogą również indukować pęknięcia pojedynczej lub podwójnej nici (DNA), prowadzące ogólnie do niestabilności genomowej (Coluzzi E i wsp., 2014).
Wiele badań wykazało związek między stresem oksydacyjnym a skracaniem telomerów, skutkującym starzeniem się komórek i organizmu (Boonekamp JJ i in., 2017) (von Zglinicki T, 2002) (Kawanishi S i Oikawa, 2004) (Richter T i von Zglinicki T, 2007) (Griffin CS, 2002). Szczególne znaczenie mają badania pokazujące bezpośrednio skracanie telomerów przez dodanie utleniacza zużywającego glutation (głównego przeciwutleniacza organizmu) (Cattan V i wsp., 2008).
To skrócenie telomerów obserwuje się u pacjentów z Covid-19 o ciężkim przebiegu, zarówno jako powiązany czynnik ryzyka (Froidure A i wsp., 2021), jak i jako konsekwencję choroby. U tych pacjentów po chorobie (Mongelli A i wsp., 2021) występuje podwyższony wiek biologiczny (który odzwierciedla dokładny stan fizjologiczny lub funkcjonalny osobnika). Ponadto, stężenie produktów utleniania guaniny (8-oksoG) w osoczu wydaje się być związane ze śmiertelnością (Lorente L i wsp., 2021)[4].
W innych chorobach związanych ze stresem oksydacyjnym również obserwuje się skracanie telomerów; zjawisko to jest skorelowane z wiekiem (Harley CB et al., 1990) (Starr JM et al., 2008) i występuje w stanach patologicznych takich jak zespół metaboliczny (który charakteryzuje się czynnikami klinicznymi takimi jak otyłość, dyslipidemia, nadciśnienie tętnicze, hiperglikemia i insulinooporność) (Gavia-García G i wsp., 2021), cukrzyca (Wang J i wsp., 2016) (Salpea KD i wsp., 2010), choroba Parkinsona (Watfa G i wsp., 2011). Jak widać, wszystkie te czynniki to choroby współistniejące.
Związek między starzeniem się a szczepionkami przeciwko Covid-19
W czerwcu 2021 r. Di Fragana i wsp. opisali w preprincie na BioRXiv, że podczas starzenia uszkodzenie DNA (skrócenie telomerów) stymuluje transkrypcję receptora ACE2, wykorzystywanego przez SARS-CoV-2, co potwierdza wyniki innych badań. Wiadomo, że zakażenie koronawirusem zespołu ostrej niewydolności oddechowej 2 (SARS-CoV-2) występuje częściej u osób starszych, u których występują również cięższe objawy i większe ryzyko hospitalizacji i zgonu. W badaniu autorzy wykazali, że ekspresja enzymu ACE2 (enzym konwertujący angiotensynę 2), który jest komórkowym receptorem SARS-CoV-2, wzrasta wraz ze starzeniem się w płucach myszy i człowieka. Jest to odpowiedź na skrócenie lub dysfunkcję telomerów w komórkach ssaków oraz w modelach mysich. Wzrost ten jest regulowany na poziomie transkrypcji, a aktywność ACE2 zależy od odpowiedzi na uszkodzenie DNA (ang. DDR – DNA damage response).
Autorzy doszli do wniosku, że podczas starzenia skrócenie telomerów poprzez aktywację DDR powoduje podwyższenie poziomu ACE2, komórkowego receptora SARS-CoV-2, co sprawia, że osoby starsze są prawdopodobnie bardziej wrażliwe na zakażenie.
Praca przed recenzją Gueudes z maja 2021 r. dotycząca porównania RNA białka kolca SARS-CoV-2 i telomerazy (enzymu, który dodaje telomery na końcu chromosomów) pozwala wyjaśnić przyspieszone starzenie się komórek pęcherzyków płucnych w ciężkich przypadkach COVID-19 oraz umożliwia wyciąganie wniosków dotyczących terapii informacyjnym RNA (zawartym w stosowanych na masową skalę pseudo-szczepienionkach) oraz postawienie szeregu pytań dotyczących związków między stanem po zaszczepieniu i po przejściu Covid-19. Telomeraza jest odwrotną transkryptazą, a autor przedstawia następujące wyjaśnienie, niepoddane jeszcze recenzji innych badaczy – „Struktura hTR [ tzn. RNA telomerazy] w kompleksie telomerazy zaangażowanym w wytwarzanie telomerów jest zwykle chroniona przed zawłaszczeniem przez obcy RNA i istnieje mechanizm kontrolujący włączanie RNA do telomerazy. Ale gdy w komórce obecna jest duża ilość obcego RNA, montaż telomerazy może być utrudniony.”
Przypomnijmy, że w 2003 roku Scholes i in. w czasopiśmie PNAS wykazali już, że erozja telomerów powoduje aktywację retrotranspozonów, a zatem odwrotna transkryptaza prawdopodobnie nie byłaby konieczna do wyjaśnienia, w jaki sposób RNA szczepionki może utrudniać montaż telomerazy i zaburzać homeostazę genomiczną.
Czy stres oksydacyjny indukowany przez szczepienie mRNA (Pfizer, Moderna) jest również odpowiedzialny za skracanie telomerów?
Białko kolca w szczepionkach również wywołuje stan zapalny i stres oksydacyjny, wiążąc się z receptorami ACE2 znajdującymi się w całym ciele (Lesgards JF, 2021).
Biorąc pod uwagę nasilenie obserwowanych skutków ubocznych oraz fakt, że mechanizmy biochemiczne są częściowo podobne, można postawić hipotezę, że szczepionki mRNA mogą utleniać guaniny w DNA i, częściowo, także telomery. Wiemy, że po szczepieniu dochodzi do wytwarzania stanu zapalnego, wzmacniającego reakcję immunologiczną i produkcję przeciwciał, a jeśli dodamy do tego działanie prooksydacyjne (jedno nie obejdzie się bez drugiego), indukowane przez białko kolca i mogące trwać co najmniej 15 dni (Ogata AF i wsp., 2021), mamy środowisko bardzo sprzyjające utlenianiu zasad DNA, z których najbardziej wrażliwą jest guanina, zwłaszcza na telomerach.
W istocie, badanie wykazało, że szczepienie szczepionką Pfizer doprowadziło do wzrostu poziomu stresu oksydacyjnego (ocenianego na podstawie pomiaru glutationu), który powrócił do normy po 14 dniach (Ntouros PA i wsp., 2021). Okres ten jest jednak wystarczający, aby spowodować uszkodzenie telomerów.
Ten stres oksydacyjny wywołany szczepieniem stwarza również inny problem, którym jest niestabilność mRNA samych szczepionek! Co bardzo zaskakujące, mRNA szczepionek Pfizer i Moderna zostało wzbogacone o więcej cząsteczek guaniny! Ma to na celu zwiększenie translacji RNA, kodującego białko kolca: rzeczywiście, jeśli zbadamy sekwencję nukleotydową genu białka kolca wirusa SARS-CoV-2 i porównamy ją z sekwencją kodującą białko kolca szczepionki, znajdziemy między nimi wiele różnic, które jednak nie wpływają na produkt translacji (ponieważ są to kodony synonimiczne, tzn. kodujące ten sam aminokwas). Te zmiany w sekwencji nukleotydów zostały wprowadzone przez badaczy, aby szczepionka była bardziej skuteczna (w miarę możliwości zastąpiono inne zasady zasadami G, aby zwiększyć skuteczność translacji). https://www.pedagogie.ac-nice.fr/svt/?p=2967.
Jednakże tak, jak producenci nie mogą zignorować toksyczności znanego od dziesięciu lat białka kolca, tym bardziej nie wolno im zignorować niestabilności (skłonności do utleniania) guaniny!
Zaskakujące jest zatem to, że żaden z organów regulacyjnych odpowiedzialnych za ocenę wniosków aplikacyjnych dotyczących pozwolenia na dopuszczenie do obrotu tych szczepionek (w szczególności FDA i EMA), znając wrażliwość telomerów i DNA na stres oksydacyjny, nie zażądał badania toksyczności genowej (genotoksyczności).
Wyciąg z raportu EMA dotyczącego Comirnaty (szczepionka Pfizer): „Genotoksyczność: Nie dostarczono badań genotoksyczności. Jest to dopuszczalne, ponieważ składniki obecne w preparacie szczepionki to lipidy i RNA, które nie powinny mieć potencjału genotoksycznego (EMA, 2021) ”.
Z punktu widzenia nauki i bezpieczeństwa pacjentów można to uznać za nieodpowiedzialne.
Czy białko kolca ze szczepionek RNA jest bardziej szkodliwe niż białko kolca wirusa SARS-CoV-2?
Na podstawie poniższych trzech eksperymentalnych oraz kolejnych teoretycznych wyjaśnień na to pytanie można odpowiedzieć twierdząco. „Stażyści bioniki” myśleli, że uczynią RNA szczepionek bardziej stabilnym poprzez dodanie do niego więcej zasad G w taki sposób, aby nie zmodyfikować powstających aminokwasów, co było możliwe dzięki temu, że w uniwersalnym kodzie genetycznym, kilka kombinacji złożonych z trzech nukleotydów (tzn. kodonów) koduje ten sam aminokwas. Niestety, w kontekście szczepionkowego RNA prowadzi to do diametralnie odmiennych wyników, ponieważ kodony zawierające więcej guaniny są bardziej niestabilne.
1 – Artykuł „zespół mimikry Covid-19 wywołany przez szczepionkę” (Marschalek et al., 2021) pokazuje, w jaki sposób to dodanie zasad G w białku kolca RNA szczepionki może powodować zmiany w ramce odczytu kodonów, a zatem [powodować odczytanie części aminokwasów w sekwencji jako innych w czasie translacji kodu genetycznego poprzez przesunięcie miejsca rozpoczęcia odczytywania złożonej z trzech elementów sekwencji] co może ostatecznie prowadzić do zdarzeń zakrzepowo-zatorowych u pacjentów zaszczepionych szczepionkami na Covid-19.[5]
2 – Ponadto wykazano, w jaki sposób ten nadmiar zasad G w RNA białka kolca szczepionek upraszcza konstrukcję tego białka, całkowicie eliminując z niej metastruktury. Dzieje się tak ze względu na zaburzenie stosunku UA do CG, który w białku wirusowym jest zgodny ze złotą proporcją, określoną przez Fibonacciego . W wirusie dochodzi do sytuacji odwrotnej – złożoność i liczba metastruktur Fibonacciego w wariantach rośnie z upływem czasu. W uproszczeniu oznacza to, że RNA szczepionek jest tylko stosem nukleotydów bez kręgosłupa stabilizującego megastrukturę na średnim i odległym dystansie, podczas gdy struktura RNA wariantów staje się z dnia na dzień coraz bardziej wytrzymała i spójna (Perez JC 2021).
3 – Ta niespójność została zobrazowana na poniższym rysunku jako rodzaj tzw. „fraktalnej chropowatości”. Niestabilność i nieharmonijność RNA kodującego białko kolca szczepionki (w szczególności Pfizera) jest istotnie większa niż RNA kodującego białko kolca wirusa, co zademonstrowano tzw. metodą master method.
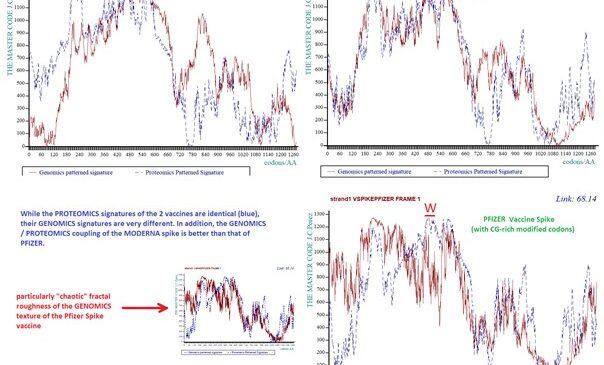
Rysunek — Nieregularna fraktalna chropowatość białka kolca powstałego pod wpływem szczepionek Pfizer i Moderna
Wyniki badań
Badania sugerują, że telomery i centromery mogą również mieć wpływ na równowagę (dostrojenie) zarówno na poziomie chromosomu, jak i całego genomu człowieka.
Od publikacji jego pierwotnej wersji w 2003 r., przeanalizowano i opublikowano kilka kolejnych, coraz bardziej precyzyjnych wersji całego ludzkiego genomu. Jednak ze względów technicznych związanych z ich powtarzalnym i pozornie wysoce zbytecznym charakterem, telomery i centromery nie były sekwencjonowane w żadnej z tych wersji. Dopiero w tym roku, tj. w 2021, opublikowano wersję zawierającą telomery.
Podczas analiz poprzednich wersji 3,5 miliarda par zasad TCAG ludzkiego genomu opublikowano dwa niezwykłe odkrycia:
1 – Pierwsze na poziomie ludzkiego chromosomu sugerujące, że erozja telomerów mogłaby wpłynąć na ogólną równowagę w skali całego chromosomu: demonstracja „cyfrowych fal stojących” na podstawie analizy sekwencji nukleotydów każdego chromosomu (każdy chromosom charakteryzuje się okresem rezonansu wyrażonym jako liczba nukleotydów, na przykład 34 dla całego chromosomu 4 (Perez JC. 2018).
2 – Drugie na poziomie całego ludzkiego genomu, gdzie w 2010 roku wykazano, że zbiory trójelementowych kodonów całego genomu ludzkiego, rzutowane według pozycji każdego z 64 kodonów w tabeli uniwersalnego kodu genetycznego, muszą przestrzegać pewnego rodzaju „cyfrowego optimum” (Perez JC. 2010). To optimum zostało z czasem udoskonalone dzięki analizom coraz bardziej precyzyjnych wersji ludzkiego genomu (2003, 2005 i …).
W tych dwóch artykułach zademonstrowano również, w jaki sposób delecje w jednym chromosomie, związane z niektórymi nowotworami, były wystarczające, aby zaburzyć równowagę w skali całego genomu.
Uzasadnione jest zatem myślenie, że degradacja telomerów może również zaburzyć GLOBALNĄ równowagę nukleotydową całego genomu w sposób analogiczny do obserwowanego w delecjach związanych z nowotworami. (Zobacz raki prostaty i piersi oraz raki mózgu – glejaka wielopostaciowego i nerwiaka zarodkowego).
Wreszcie, jak wykazano wcześniej dla badania dotyczącego usuwania fragmentów chromosomu związanych z powstawaniem nowotworów, uważamy, że ta przyspieszona „erozja” telomerów, prawdopodobnie powiązana z białkiem kolca wirusa, ale także z białkiem kolca szczepionek, może wpłynąć na równowagę w skali każdego chromosomu, a następnie całego genomu.
Wnioski
Te badania i obserwacje dostarczają kluczowych informacji o chorobie i fundamentalnej odpowiedzi na pytanie o większą podatność na tę chorobę osób starszych lub z niedoborem odporności. Rzeczywiście, wraz z wiekiem telomery ulegają degradacji, wpływając na reprodukcję komórek. Uważa się, że SARS-CoV-2 powoduje biologiczne starzenie się lub zwiększenie wieku biologicznego poprzez przyspieszenie skracania telomerów.
Pytanie, które można słusznie zadać, brzmi: czy białko kolca w szczepionkach (Pfizer, Moderna itp.) wywiera biologiczny wpływ na receptor ACE2 (blokując lub aktywując go) i hamuje korzystne działanie ochronne telomerów, a tym samym aktywuje starzenie się?
W takim wypadku istniałby bezpośredni związek między chorobą a działaniem odwrotnej transkryptazy, będącej częścią ludzkiej maszynerii komórkowej. Żadna tradycyjna szczepionka nigdy nie miała na celu wywołanie takiego efektu biologicznego.
W walce z SARS-COV-2 istotne wydają się dwie strategie, które należy realizować jednocześnie:
1 – Zapobieganie zachorowaniom – wykorzystanie w podejściu terapeutycznym znanych metod zapobiegania zakażeniom, wczesnego leczenia i „sprawdzonych szczepień”. Zastosowanie działań profilaktycznych obejmujących również zdrowy styl życia, zbilansowaną dietę, aktywność fizyczną, wystarczający odpoczynek i interakcje społeczne. Mens sana in corpore sano (w zdrowym ciele zdrowy duch) – to stwarza najlepsze warunki do walki z wirusami i bakteriami.
2 – Zapobieganie ciężkiemu przebiegowi choroby – wymaga to przede wszystkim pełnego zrozumienia wirusa, sposobu jego działania oraz konsekwencji choroby dla zaatakowanych przez nią narządów.
Do tej pory zarządzanie kryzysem na poziomie zdrowia publicznego polegało na wstrzykiwaniu substancji nadal będących w trakcie badań, w momencie publikacji tego artykułu w fazie 3, dla których definicja słowa „szczepionka” musiała zostać zmodyfikowana przez samą WHO. Ponadto przyjmuje się, że wstrzyknięcie szczepionki w technologii mRNA powoduje zwiększoną produkcję białka kolca, ale nie zmniejsza transmisji wirusa (szczepienie Pfizerem wykazuje jedynie 42% skuteczności wobec wariantu delta). Przeprowadzanie masowych akcji szczepień tworzy dobre warunki do powstawania i rozprzestrzeniania się wariantów wirusa, wobec których odporność poszczepienna jest bezskuteczna. W krajach, w których populacje zaszczepiły się masowo, opublikowane przez władze dane wykazują, że wysoki odsetek hospitalizowanych to osoby w pełni zaszczepione. Należy zauważyć, że do tej pory instytucje francuskie nie zgłaszają tych samych obserwacji; można to częściowo wytłumaczyć opóźnieniem w rozpoczęciu kampanii szczepień (+ 2 miesiące w porównaniu na przykład z Izraelem).
Profesor Montagnier mówi: „aby zapobiec starzeniu się, weź antyoksydanty! Mówię to od 30 lat, a teraz dodałbym jeszcze: weź je, żeby nie utracić swoich telomerów”.
Pojawia się kilka pytań dotyczących wirusa:
1 – Czy lepiej jest zakazić się chorobą losowo i rozwinąć naturalną odpowiedź immunologiczną, czy też wypróbować na sobie szczepionkę, ponosząc wiele skutków ubocznych zgłaszanych przez nadzór nad bezpieczeństwem farmakoterapii, a także narazić się na ryzyko przyspieszonego starzenia się komórek?
2 – Czy zwiększenie wieku biologicznego u pacjentów z Covid-19 i osób zaszczepionych jest takie samo, czy jedno z nich prowadzi do bardziej zaawansowanych zmian? Na tym etapie nikt nie jest w stanie udzielić precyzyjnej odpowiedzi na te pytania.
W każdym razie wirus ten powoduje wzrost wieku biologicznego u osób, które zarażą się chorobą, czego efekt jest prawdopodobnie wzmocniony przez podanie szczepionki. Wraz ze spadkiem jej skuteczności w walce z zakażeniami, konieczne jest zatem zapobieganie ciężkiemu przebiegowi choroby u pacjentów i dlatego konieczne jest wczesne leczenie.
Pozwalając chorobie na niekontrolowany postęp przez kilka pierwszych dni (nie stosując leków) i uznając szczepionki za jedyne rozwiązanie, stwarza się ryzyko skrócenia życia zarówno dorosłych, jak i dzieci. Czy w czasie, gdy kobiety i mężczyźni starają się starzeć w najlepszych możliwych warunkach i pozostać młodymi jak najdłużej, chcemy ryzykować regularne zastrzyki, które zrujnują wszystkie te wysiłki? W obliczu chęci zaszczepienia populacji dzieci, której SARS-CoV-2 nie dotyka, lekarstwo nie powinno być gorsze od choroby.
W świetle odczuć niektórych pacjentów, którzy zarazili się Covid-19 i niektórych zaszczepionych osób, które miały wrażenie, że „przeżyły dziesięć lat na raz”, czyżby nauka po raz kolejny, we właściwym czasie, przyniosła dowód na korzyści wynikające ze wczesnego leczenia? Ostatnim krokiem, przed którym część się nie zawaha, jest zadeklarowanie, że zwiększenie wieku biologicznego doprowadzi do skrócenia oczekiwanej długości życia.
Autorzy tej analizy i forum w porządku alfabetycznym: Xavier Azalbert, Anne-Typhaine Bouthors, Michel Brack, Dominique Cerdan, Walter Chesnut, Gérard Guillaume, Jean-François Lesgards, Luc Montagnier, Jean-Claude Perez.
Podziękowania dla wielu członków Kolektywu Obywatelskiego za korektę.
[1] Tekst opublikowany w dziale naukowym France Soir, pt.: Le SARS-COV2 accélérerait l’âge biologique, por. https://www.francesoir.fr/opinions-tribunes/le-sars-cov2-accelererait-lage-biologique, (2021-09-01). Za wyrażenie zgody na tłumaczenie oraz publikację na stronie Ordo Medicus wyrażamy podziękowanie Redakcji France Soir; Copyright ©by France Soir 2021. W oryginale tekst opatrzony jest uwagą: Cet espace d’opinion permet la libre expression des idées et d’engendrer le débat. Les articles et vidéos publiés dans cette rubrique peuvent parfois ne pas faire consensus (Ta « przestrzeń opinii » pozwala na swobodne wyrażanie idei i prowokuje debatę. Artykuły i filmy publikowane w tej sekcji mogą czasami nie osiągnąć konsensusu.).
[2] in. SARS-CoV-2 przyspiesza starzenie się
[3] Por. https://pl.wikipedia.org/wiki/Układ_renina–angiotensyna–aldosteron (2021-09-25).
[4] Por. https://link.springer.com/article/10.1007/s11239-020-02190-9 – link do badania Lorente L i wsp., dotyczącego czynników prognostycznych dla wystąpienia zatorowości płucnej u pacjentów z zakażeniem SARS-CoV-2.
[5] Por. https://www.researchsquare.com/article/rs-558954/v1 – link do artykułu Marschalek i wsp., dotyczącego zdarzeń niepożądanych podczas transkrypcji sekwencji kodującej białko kolca w szczepionce wektorowej AstraZeneca, skutkujących utratą części potrzebnych informacji w trakcie splicingu w jądrze komórkowym ludzkiej komórki eukariotycznej – oraz zmianą struktury powstającego białka kolca.
za: ordomedicus.org
fot. Vieux tel Homère… FS





![Oszustwo testów PCR – zyskajmy wiedzę i stosujmy ją w praktyce w kolejnym sezonie przeziębieniowym – DR Z. HAŁAT [WIDEO]](https://politykapolska.eu/wp-content/uploads/2020/04/covid-19-PCR-Test-2-218x150.jpg)



![Relacja z konferencji: Depopulacja Polski – jak przeciwdziałać? Szanse i zagrożenia dla przyszłych pokoleń Polaków [cz.II]](https://politykapolska.eu/wp-content/uploads/2026/05/Rodzina-5-osobowa_CzasDlaMilosci-100x70.png)
![Relacja z konferencji [cz.I]: Depopulacja Polski – jak przeciwdziałać? Szanse i zagrożenia dla przyszłych pokoleń Polaków](https://politykapolska.eu/wp-content/uploads/2026/04/depopulacja-Polski-plakat-1-FB-INSTA-100x70.png)










![W. Engdahl: „Skandal koronawirusowy wychodzi na jaw – w Niemczech pani Merkel” + w Polsce pana Morawieckiego [ENGLISH]](https://politykapolska.eu/wp-content/uploads/2020/12/PCR-Test-na-Covida-100x70.jpg)